Strukturuntersuchungen an Auxin-Phytohormonen.
 |
English version.
|
| © |
Copyright-Hinweis. |
 |
Übersicht. |
Strukturuntersuchungen an Auxin-Phytohormonen. |
|
Die Potenzialfläche von
4-Chlorindol-3-essigsäure
enthält vier symmetrieeindeutige lokale Minima mit einer
cis-Orientierung der COOH-Gruppe, deren Geometrien über diesem
Absatz in der Reihenfolge ihrer Energien gezeigt sind.
Die 6-31G*-optimierten
T1/T2-Werte
und die relativen Energien sind in der Tabelle zusammengefasst.
So wie im Falle der unsubstituierten Indol-3-essigsäure (IAA)
ist das globale Minimum (A)
spiegelsymmetrisch und durch eine schwache
C=O···H-C2-Wasserstoffbrücke
stabilisiert. Im Gegensatz zu IAA gibt es für die Konformere mit
gewinkelter Seitenkette nur zwei verschiedene Orientierungen für die
COOH-Gruppe, für die sich die
entsprechenden Torsionswinkel um etwa 180° unterscheiden; diese beiden
Konformere sind hinsichtlich der Energie zweit- und drittgereiht.
Das vierte symmetrieeindeutige lokale Minimum (D) ist
nicht nur wegen seiner hohen relativen Energie bemerkenswert, sondern auch
weil es eine T1/T2-Position besetzt,
die in unsubstituierter IAA einem Sattelpunkt
entspricht. Des weiteren ist D kein stabiles Konformer:
die kleinste Potenzialbarriere (in der Reaktion zu A)
beträgt nur 0,452 kJ/mol und liegt damit unter der
Energie der Nullpunktsschwingung der entsprechenden Mode
(für die die Berechnung
eine unskalierte, harmonische Frequenz von 103,53 cm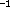 ergibt).
ergibt).
| Konformer | T1 | T2 | E [kJ/mol] |
|---|---|---|---|
| A | 0,000° | 0,000° | 0,000 |
| B | 105,623° | -14,059° | 2,683 |
| C | 110,991° | 162,977° | 6,316 |
| D | 5,789° | 115,002° | 8,988 |
Diese vier Energieminima und ihre Enantiomere sind durch ein Netzwerk von Reaktionswegen verbunden, welches die folgenden Verbindungen enthält (Kleinbuchstaben kennzeichnen die Spiegelbilder): A-B, A-b, A-C, A-c, A-D, A-d, B-c, B-D, C-D und D-d. Bemerkenswert ist, dass es keine direkte Reaktion zwischen B und C gibt, die COOH-Gruppe also in keinem dieser Konformere frei drehbar ist. Ausgehend von B oder C ist eine Rotation der COOH-Gruppe stets an eine Drehung der Essigsäureseitenkette gekoppelt.
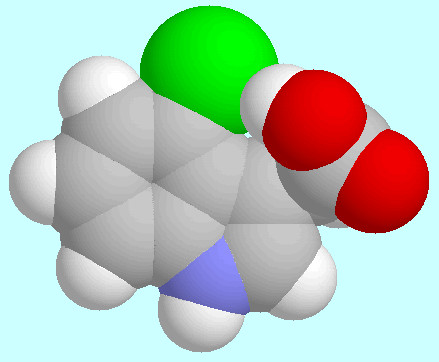
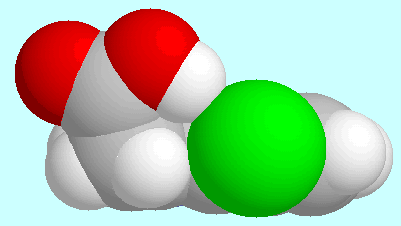 4-Cl-IAA kann eine
O-H···Cl-Wasserstoffbrücke bilden, die einen
achtgliedrigen Ring schließt. Die Geometrie dieses
wasserstoffbrückengebundenen Konformers ist, aus zwei verschiedenen
Richtungen gesehen, neben diesem Absatz gezeigt. Wegen der starren Natur
des Indolkerns ist die resultierende Wasserstoffbrücke
deutlich schwächer als diejenigen in
4-Cl-IAA kann eine
O-H···Cl-Wasserstoffbrücke bilden, die einen
achtgliedrigen Ring schließt. Die Geometrie dieses
wasserstoffbrückengebundenen Konformers ist, aus zwei verschiedenen
Richtungen gesehen, neben diesem Absatz gezeigt. Wegen der starren Natur
des Indolkerns ist die resultierende Wasserstoffbrücke
deutlich schwächer als diejenigen in
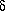 -Aminopentansäure oder
-Aminopentansäure oder
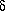 -Hydroxypentansäure, welche ebenfalls zu
achtgliedrigen Ringen führen:
die relative 6-31G*-Energie dieses Konformers beträgt 24,914 kJ/mol,
die Bindungsordnung der Wasserstoffbrücke nur 0,027.
-Hydroxypentansäure, welche ebenfalls zu
achtgliedrigen Ringen führen:
die relative 6-31G*-Energie dieses Konformers beträgt 24,914 kJ/mol,
die Bindungsordnung der Wasserstoffbrücke nur 0,027.