Intramolekulare Wasserstoffbrücken in Aminosäuren.
 |
English version. |
| © |
Copyright-Hinweis. |
 |
Übersicht. |
Intramolekulare Wasserstoffbrücken in Aminosäuren. |
|
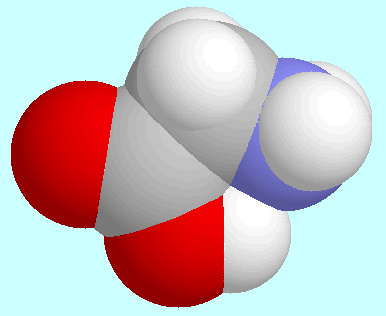 Glycin
bildet ein Konformer mit einer intramolekularen
O-H···N Wasserstoffbrücke.
Mit split-valence Basissätzen ist dieses Konformer spiegelsymmetrisch,
während Basissätze mit Polarisationsfunktionen eine ähnliche,
aber leicht unsymmetrische Geometrie ergeben.
In diesem Fall gibt es daher genau genommen zwei lokale Minima in der
Potenzialfläche, aber die Barriere zwischen diesen ist extrem
niedrig.
Glycin
bildet ein Konformer mit einer intramolekularen
O-H···N Wasserstoffbrücke.
Mit split-valence Basissätzen ist dieses Konformer spiegelsymmetrisch,
während Basissätze mit Polarisationsfunktionen eine ähnliche,
aber leicht unsymmetrische Geometrie ergeben.
In diesem Fall gibt es daher genau genommen zwei lokale Minima in der
Potenzialfläche, aber die Barriere zwischen diesen ist extrem
niedrig.
Dieses wasserstoffbrückengebundene Konformer ist nicht das globale Minimum der Potenzialfläche, was im Bereich der Quantenchemie Geschichte gemacht hat: es wurde nämlich zuerst im Gasphasen-Mikrowellenspektrum als die stabilste Form identifiziert, weil die Intensitäten seiner Signale so hoch sind, wohingegen die ab initio Berechnungen eine spiegelsymmetrische Form ohne Wasserstoffbrücken als globales Minimum ergaben.
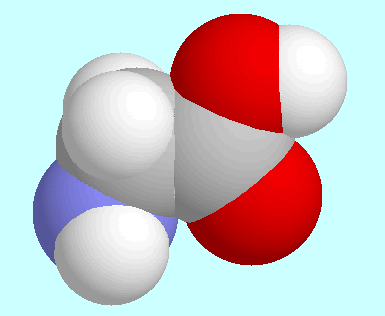 Auf Grund der Vorhersagen für die Rotationskonstanten dieser
berechneten Form wurden die entsprechenden Signale dann auch im
Mikrowellenspektrum identifiziert. Die scheinbare Differenz zwischen
Theorie und Experiment fand dann eine simple Erklärung: die
höheren Intensitäten der wasserstoffbrückengebundenen Form
waren nicht durch höhere Besetzung, also niedrigere Energie,
verursacht, sondern durch das wesentlich größere Dipolmoment,
das seine Ursache eben in der intramolekularen Wasserstoffbrückenbindung
hat.
Seit dieser Episode war Glycin Gegenstand zahlreicher Studien und diente auch
wiederholt als Testmolekül für neue quantenchemische Verfahren.
Auf Grund der Vorhersagen für die Rotationskonstanten dieser
berechneten Form wurden die entsprechenden Signale dann auch im
Mikrowellenspektrum identifiziert. Die scheinbare Differenz zwischen
Theorie und Experiment fand dann eine simple Erklärung: die
höheren Intensitäten der wasserstoffbrückengebundenen Form
waren nicht durch höhere Besetzung, also niedrigere Energie,
verursacht, sondern durch das wesentlich größere Dipolmoment,
das seine Ursache eben in der intramolekularen Wasserstoffbrückenbindung
hat.
Seit dieser Episode war Glycin Gegenstand zahlreicher Studien und diente auch
wiederholt als Testmolekül für neue quantenchemische Verfahren.
 -Alanin.
-Alanin.