Intramolekulare Wasserstoffbrücken in Aminosäuren.
 |
English version. |
| © |
Copyright-Hinweis. |
 |
Übersicht. |
Intramolekulare Wasserstoffbrücken in Aminosäuren. |
|
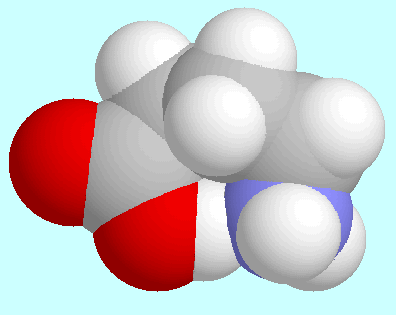
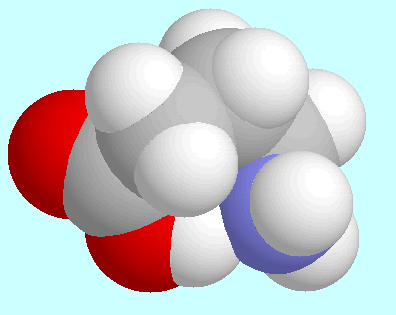
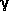 -Aminobuttersäure ist physiologisch
wichtig als inhibitorische
Neurotransmittersubstanz; aus diesem Grund
hat sie eine oft verwendete Abkürzung erhalten: GABA (= Gamma Amino
Butyric Acid). Die Neutralform von GABA bildet insgesamt vier Konformere mit
O-H···N
Wasserstoffbrücken, die zwei Enantiomerenpaare bilden.
Eines dieser Enantiomerenpaare hat eine Geometrie vom Umschlagtyp,
in der die COOH-Gruppe, das Stickstoffatom, und die Kohlenstoffatome
-Aminobuttersäure ist physiologisch
wichtig als inhibitorische
Neurotransmittersubstanz; aus diesem Grund
hat sie eine oft verwendete Abkürzung erhalten: GABA (= Gamma Amino
Butyric Acid). Die Neutralform von GABA bildet insgesamt vier Konformere mit
O-H···N
Wasserstoffbrücken, die zwei Enantiomerenpaare bilden.
Eines dieser Enantiomerenpaare hat eine Geometrie vom Umschlagtyp,
in der die COOH-Gruppe, das Stickstoffatom, und die Kohlenstoffatome
 und
und 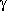 ungefähr in einer Ebene liegen; das andere
hat die Kohlenstoffatome
ungefähr in einer Ebene liegen; das andere
hat die Kohlenstoffatome 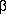 und
und 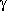 außerhalb der Ebene, die durch die
COOH-Gruppe, das Kohlenstoffatom
außerhalb der Ebene, die durch die
COOH-Gruppe, das Kohlenstoffatom  und das Stickstoffatom gebildet wird.
Die Wasserstoffbrücken sind in diesen beiden Paaren unterschiedlich
stark: stärker im erstgenannten Paar, schwächer im letztgenannten.
Die Überlappung der Kalotten in den Abbildungen zeigt die
unterschiedliche Stärke sehr gut.
und das Stickstoffatom gebildet wird.
Die Wasserstoffbrücken sind in diesen beiden Paaren unterschiedlich
stark: stärker im erstgenannten Paar, schwächer im letztgenannten.
Die Überlappung der Kalotten in den Abbildungen zeigt die
unterschiedliche Stärke sehr gut.
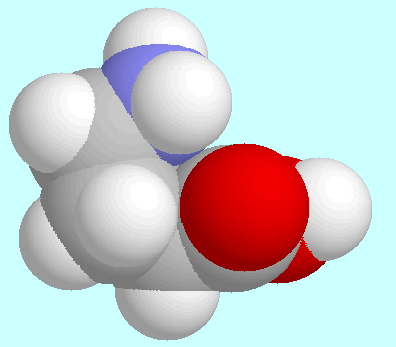 So wie in Glycin und
So wie in Glycin und 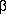 -Alanin sind die wasserstoffbrückengebundenen
Konformere nicht die globalen Minima der Potenzialfläche.
Die Struktur des globalen Minimums von GABA ist analog zu der von
-Alanin sind die wasserstoffbrückengebundenen
Konformere nicht die globalen Minima der Potenzialfläche.
Die Struktur des globalen Minimums von GABA ist analog zu der von
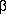 -Alanin: die
COOH-Gruppe und die Kohlenstoffatome
-Alanin: die
COOH-Gruppe und die Kohlenstoffatome  und
und
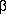 liegen in einer Ebene, das Kohlenstoffatom
liegen in einer Ebene, das Kohlenstoffatom 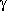 ragt aus dieser heraus,
und die Aminogruppe ist zur Carbonylgruppe hin orientiert.
So wie in
ragt aus dieser heraus,
und die Aminogruppe ist zur Carbonylgruppe hin orientiert.
So wie in 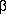 -Alanin
ist die daraus resultierende Wechselwirkung zwischen Carbonylsauerstoffatom
und dem Wasserstoffatom der Aminogruppe keine Wasserstoffbrücke.
-Alanin
ist die daraus resultierende Wechselwirkung zwischen Carbonylsauerstoffatom
und dem Wasserstoffatom der Aminogruppe keine Wasserstoffbrücke.
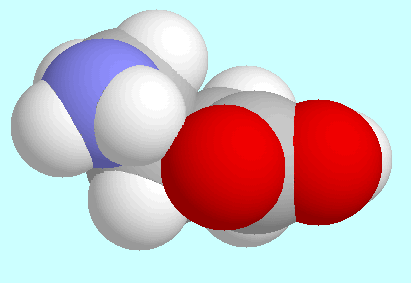 Die Potenzialfläche von GABA enthält 62
symmetrie-eindeutige Energieminima; unter diesen ist ein einziges, das
eine N-H···O=C Wasserstoffbrücke ausbildet. Die
Geometrie dieses hochenergetischen Konformeren, das die COOH-Gruppe in der
energetisch ungünstigen trans-Orientierung hat, ist neben diesem
Absatz gezeigt. Bemerkenswerterweise sind dieses Konformer, sein Enantiomeres
und die Konformere mit der
starken N···H-O Wasserstoffbrücke die einzigen
wasserstoffbrückengebundenen Konformere in der GABA-Potenzialfläche.
Die Potenzialfläche von GABA enthält 62
symmetrie-eindeutige Energieminima; unter diesen ist ein einziges, das
eine N-H···O=C Wasserstoffbrücke ausbildet. Die
Geometrie dieses hochenergetischen Konformeren, das die COOH-Gruppe in der
energetisch ungünstigen trans-Orientierung hat, ist neben diesem
Absatz gezeigt. Bemerkenswerterweise sind dieses Konformer, sein Enantiomeres
und die Konformere mit der
starken N···H-O Wasserstoffbrücke die einzigen
wasserstoffbrückengebundenen Konformere in der GABA-Potenzialfläche.
Analog zu 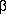 -Alanin
gibt es auch für GABA Reaktionswege, die die
O-H···N Wasserstoffbrücke intakt lassen.
Im Falle von GABA sind es zwei energetisch unterschiedliche Reaktionswege,
die die verschiedenen wasserstoffbrückengebundenen Konformere in einem
geschlossenen Zyklus
A-B-a-b-A ("a" und "b" bezeichnen die Spiegelbilder)
verbinden. Jedes dieser Konformere hat daher die "Wahl" zwischen zwei
verschiedenen wasserstoffbrückenerhaltenden Wegen.
Im Unterschied zu 3-Aminopropanol,
wo es einen analogen Reaktionszyklus gibt, haben diese Reaktionen
in GABA für die wasserstoffbrückengebundenen Konformere
jeweils die kleinsten Potenzialbarrieren.
-Alanin
gibt es auch für GABA Reaktionswege, die die
O-H···N Wasserstoffbrücke intakt lassen.
Im Falle von GABA sind es zwei energetisch unterschiedliche Reaktionswege,
die die verschiedenen wasserstoffbrückengebundenen Konformere in einem
geschlossenen Zyklus
A-B-a-b-A ("a" und "b" bezeichnen die Spiegelbilder)
verbinden. Jedes dieser Konformere hat daher die "Wahl" zwischen zwei
verschiedenen wasserstoffbrückenerhaltenden Wegen.
Im Unterschied zu 3-Aminopropanol,
wo es einen analogen Reaktionszyklus gibt, haben diese Reaktionen
in GABA für die wasserstoffbrückengebundenen Konformere
jeweils die kleinsten Potenzialbarrieren.
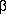 -Alanin.
-Alanin.
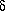 -Aminopentansäure.
-Aminopentansäure.